As titulações podem ser classificadas de várias maneiras: pela sua reação química (por exemplo, titulação ácido-base ou titulação redox), pelo método de indicação (por exemplo, titulação potenciométrica ou titulação fotométrica) e, por último, mas não menos importante, pelo seu princípio de titulação (titulação direta ou titulação indireta). Neste artigo, quero elaborar um princípio específico de titulação – a retrotitulação – que também é chamada de «titulação residual». Saiba mais sobre quando ele é usado e como você deve calcular os resultados ao usar o princípio da retrotitulação.
O que é uma retrotitulação?
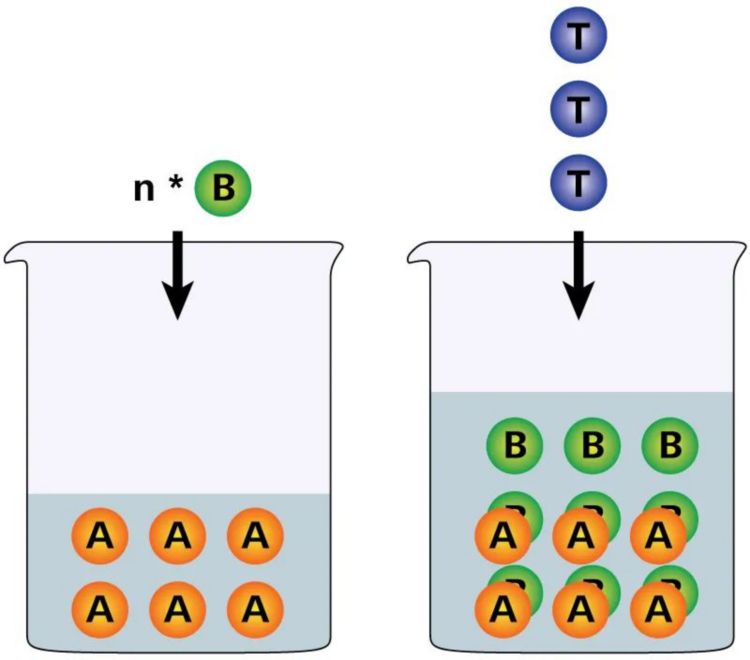
Em contraste com titulações diretas, onde o analito A reage diretamente com o titulante T, as retrotitulações são uma subcategoria das titulações indiretas. As titulações indiretas são usadas quando, por exemplo, nenhum sensor adequado está disponível ou a reação é muito lenta para uma titulação direta prática.
Durante uma retrotitulação, um volume exato de reagente B é adicionado ao analito A. Reagente B geralmente é um titulante comum. A quantidade de reagente B é escolhido de tal forma que um excesso permaneça após sua interação com o analito A. Este excesso é então titulado com titulante T. A quantidade de analito A pode então ser determinado a partir da diferença entre a quantidade adicionada de reagente B e o excesso restante de reagente B.
Como acontece com qualquer titulação, ambas as reações envolvidas devem ser quantitativas e os fatores estequiométricos envolvidos em ambas as reações devem ser conhecidos.
Quando as retrotitulações são usadas?
As titulações reversas são usadas principalmente nos seguintes casos:
- se o analito for volátil (por exemplo, NH3) ou um sal insolúvel (por exemplo, Li2CO3)
- se a reação entre o analito A e titulante T é muito lento para uma titulação direta prática
- se reações de ácido fraco – base fraca estiverem envolvidas
- quando nenhum método de indicação adequado estiver disponível para uma titulação direta
Exemplos típicos são titulações complexométricas, por exemplo alumínio com EDTA. Esta titulação direta só é viável em temperaturas elevadas. No entanto, a adição de EDTA em excesso ao alumínio e a retrotitulação do EDTA residual com sulfato de cobre permitem uma titulação à temperatura ambiente. Isto não se aplica apenas ao alumínio, mas também a outros metais.
Aprenda quais metais podem ser titulados diretamente e para quais metais a retrotitulação é mais viável em nosso programa gratuito monografia sobre titulação complexométrica.
Outros exemplos incluem o valor de saponificação e valor de iodo para gorduras e óleos comestíveis. Para o valor de saponificação, KOH etanólico é adicionado em excesso à gordura ou óleo. Após determinado tempo de refluxo para saponificar o óleo ou gordura, o excesso remanescente é retrotitulado com ácido clorídrico. O processo é semelhante para o valor de iodo, onde o excesso restante de cloreto de iodo (solução de Wijs) é retrotitulado com tiossulfato de sódio.
Para obter mais informações sobre a análise de gorduras e óleos comestíveis, consulte nosso Boletim de Aplicação gratuito correspondente AB-141.

Como é realizada uma retrotitulação?
Uma retrotitulação é realizada de acordo com o seguinte princípio geral:
- Adicionar reagente B em excesso para analisar A.
- Permitir reagente B reagir com o analito A. Isto pode exigir um certo tempo de espera ou mesmo refluxo (por exemplo, valor de saponificação).
- Titulação do excesso restante de reagente B com titulante T.
Para a primeira etapa, é importante adicionar com precisão o volume de reagente B. Portanto, é importante utilizar uma bureta para esta adição (Figura 2).
Além disso, é importante que o quantidade molar exata de reagente B é conhecido. Isto pode ser alcançado de duas maneiras. A primeira forma é realizar uma determinação em branco da mesma forma que a retrotitulação da amostra, porém omitindo a amostra. Se reagente B é um titulante comum (por exemplo, EDTA), também é possível realizar uma padronização do reagente B antes da retrotitulação.
Em qualquer caso, como padronização do titulante T é necessário. Isso nos dá os dois procedimentos gerais de análise a seguir:
Retrotitulação com branco
- Determinação do título do titulante T
- Determinação em branco (retrotitulação omitindo amostra)
- Retrotitulação da amostra
Retrotitulação com padronizações
- Determinação do título do titulante T
- Determinação do título do reagente B
- Retrotitulação da amostra
Estar ciente: como você está realizando uma retrotitulação, o volume do branco será maior que o volume do ponto de equivalência (EP), diferentemente do branco em uma titulação direta. É por isso que o volume de EP deve ser subtraído do branco ou do volume adicionado de reagente B, respectivamente.
Para obter mais informações sobre a padronização de titulantes, dê uma olhada em nosso blog sobre este tópico.
Como calcular o resultado de uma retrotitulação
Tal como acontece com as titulações diretas, para calcular o resultado de uma retrotitulação é necessário conhecer as reações estequiométricas envolvidas, além das concentrações e volumes exatos. Dependendo do procedimento de análise descrito acima é utilizado, o cálculo do resultado é ligeiramente diferente.
Para retrotitulação com branco, use a seguinte fórmula para obter um resultado em% em massa:
VEm branco: Volume do ponto de equivalência da determinação do branco em mL
VPE: Volume no ponto de equivalência em mL
cTitulante: Concentração nominal de titulante em mol/L
fTitulante: Fator de título do titulante (sem unidade)
R: Razão estequiométrica (sem unidade)
MA: Peso molecular do analito A em g/mol
euAmostra: Peso da amostra em mg
100: Fator de conversão, para obter o resultado em %
O razão estequiométrica r considera ambas as reações, analito A com reagente B e reagente B com titulante T. Se o fator estequiométrico for sempre 1, como para retrotitulações complexométricas ou o valor de saponificação, então a razão de reação também será 1. No entanto, se o fator estequiométrico para uma reação não for igual a 1, então a razão da reação deve ser determinada. A razão de reação pode ser determinada da seguinte maneira:
- Equação de reação entre A e B
- Equação de reação entre B e T
- Multiplicação dos dois quocientes de reação
Exemplo 1
Exemplo 2
Abaixo está um exemplo real de carbonato de lítio, que pode ser determinado por retrotitulação usando ácido sulfúrico e hidróxido de sódio.
O carbonato de lítio reage na proporção de 1:1 com ácido sulfúrico. Para determinar o excesso de ácido sulfúrico, são necessários dois moles de hidróxido de sódio por mol de ácido sulfúrico, resultando em uma proporção de 1:2. Isto dá uma razão estequiométrica r de 0,5 para esta titulação.
Para retrotitulação com padronização de reagente B, use a seguinte fórmula para obter um resultado em% em massa:
VB: Volume adicionado do reagente B em mL cB: Concentração nominal do reagente B em mol/L fB: Fator de título do reagente B (sem unidade) VEP: Volume no ponto de equivalência em mL cT: Concentração nominal do titulante T em mol/ L fT: Fator de título do titulante T (sem unidade) sBT: Fator estequiométrico entre o reagente B e o titulante T sAB: Fator estequiométrico entre o analito A e o reagente B MA: Peso molecular do analito A em g/mol mAmostra: Peso da amostra em mg 100:Fator de conversão, para obter o resultado em %

Os tituladores modernos são capazes de calcular automaticamente os resultados das retrotitulações. Todas as informações relativas às variáveis utilizadas (por exemplo, valor em branco) são armazenadas juntamente com o resultado para total rastreabilidade.
Para resumir:
As retrotitulações não são tão diferentes das titulações regulares e os mesmos princípios gerais se aplicam. Os seguintes pontos são necessários para uma retrotitulação:
- Conheça as reações estequiométricas entre o analito e o reagente B, bem como entre reagente B e titulante T.
- Conheça a concentração exata do seu titulante T.
- Conheça a concentração exata do seu reagente B, ou executar uma determinação em branco.
- Use parâmetros de titulação apropriados dependendo da sua análise.
Se você quiser saber mais sobre como você pode melhorar sua titulação, dê uma olhada em nosso blog abaixo, onde você pode encontrar dicas práticas sobre como melhorar suas titulações.
Como transferir a titulação manual para a titulação automática
Se você estiver não tenho certeza de como determinar a concentração exata do seu titulante T ou reagente B por padronização, então dê uma olhada em nosso artigo de blog relacionado aqui.
 Compartilhar artigo
Compartilhar artigo
