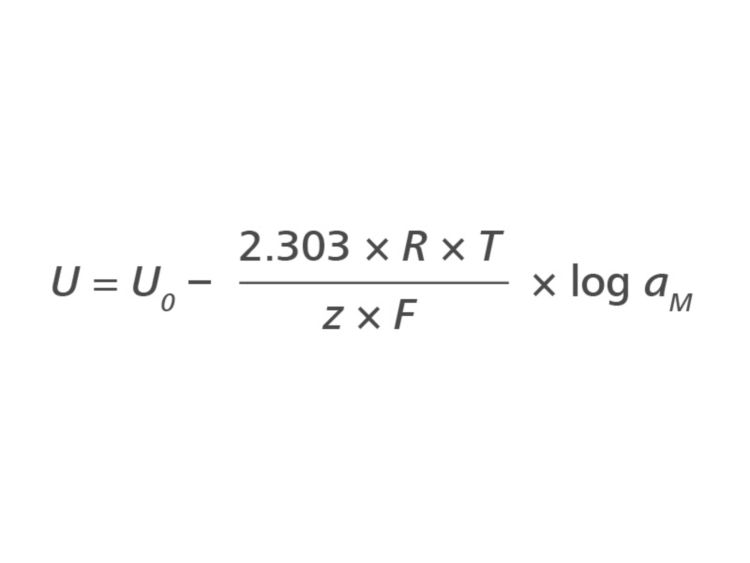Mesmo pequenas mudanças na temperatura podem impactar significativamente as medições de pH, pois as duas estão interligadas. A temperatura afeta a medição do pH de várias maneiras. Este artigo do blog abordará os motivos e discutirá como você pode lidar com os diferentes efeitos da temperatura nas medições de pH.
Clique para ir diretamente para um tópico:
- Por que a temperatura afeta o valor do pH?
- Efeitos da temperatura na medição de pH e como lidar com eles
– Escolha de um vidro de membrana apropriado
– Posicionamento correto do sensor de temperatura e do eletrodo de pH
– Eletrodos de pH combinados com sistema de referência «Long Life»
Por que a temperatura afeta o valor do pH?
A temperatura e o valor do pH estão relacionados pelo Equação de Nernst. Esta equação descreve a relação ideal entre a atividade aM de um íon de medição em solução e o potencial medido entre o eletrodo de referência e o eletrodo de medição. A temperatura influencia o Potencial de Nernst – mais frequentemente chamado de declive na medição de pH.
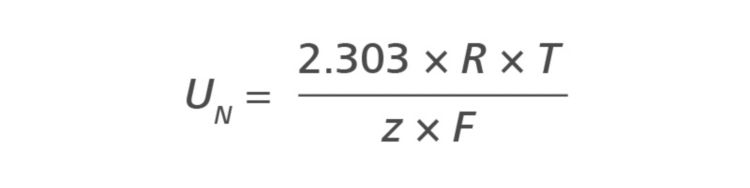
A partir disso, o declive vocêN pode ser calculado:
Uma mudança de temperatura de 1 °C corresponde a uma mudança de 0,2 mV. Colocando isto em termos relativos: uma diferença de pH de 0,01 corresponde a 0,6 mV. Portanto, é necessário levar em consideração a temperatura em todas as medições de pH. Caso contrário, nenhum resultado correto será obtido se as temperaturas de calibração e medição não forem conhecidas.
A inclinação vocêN é diferente para diferentes temperaturas. Em T = 298,16 K = 25 °C e z = 1, o declive vocêN é igual a 59,16 mV. Para outras temperaturas, um valor diferente para a inclinação vocêN é usado no Equação de Nernst. Isso é chamado de compensação de temperatura. tabela 1 lista o valor da inclinação para diferentes temperaturas.
tabela 1. Dependência da temperatura da encosta.
| Temperatura T [°C] | Declive vocêN [unidade mV/pH] |
Temperatura T [°C] | Declive vocêN [unidade mV/pH] |
|---|---|---|---|
| 0 | 54,20 | 50 | 64,12 |
| 5 | 55,19 | 55 | 65,11 |
| 10 | 56,18 | 60 | 66,10 |
| 15 | 57,17 | 65 | 67,09 |
| 20 | 58,16 | 70 | 68,08 |
| 25 | 59,16 | 75 | 69,07 |
| 30 | 60,15 | 80 | 70,07 |
| 35 | 61,14 | 85 | 71,06 |
| 37 | 61,54 | 90 | 72,05 |
| 40 | 62,13 | 95 | 73,04 |
| 45 | 63,12 | 100 | 74,03 |
Os medidores de pH modernos incluem uma função para fins de compensação de temperatura. Isto significa que assim que um sensor de temperatura é conectado ao medidor de pH, a dependência da temperatura da inclinação vocêN é automaticamente considerado e corrigido. Medir a temperatura não só ajuda a garantir medições precisas de pH, mas também garante a conformidade com as diretrizes GLP/ISO que exigem o registro da temperatura para todas as medições.
Efeitos da temperatura na medição de pH e como lidar com eles
O valor do pH é provavelmente o parâmetro mais comumente medido em química analítica. Influencia as características do produto, as reações químicas e bioquímicas e os processos fisiológicos, entre outras coisas. Freqüentemente, condições ambientais consistentes são necessárias para resultados de medição precisos.
Em alguns casos, as mudanças de temperatura não podem ser evitadas. Por exemplo, a simples abertura de uma porta pode causar uma alteração na temperatura ambiente. Mesmo quando se trabalha em ambientes com ar condicionado, podem ocorrer reações exotérmicas resultando num aumento de temperatura. As causas das flutuações de temperatura não poderiam ser mais variadas – portanto, esta seção lhe dará algumas dicas de preparação. Siga-os para minimizar ou até mesmo eliminar possíveis efeitos relacionados à temperatura antes de iniciar sua calibração/medição de pH.
Escolha de um vidro de membrana apropriado
Para cobrir medições de pH em uma ampla variedade de amostras, a Metrohm oferece Eletrodos de pH com diferentes tipos de membrana de vidro.

No temperaturas mais altas o eletrodo de pH envelhece mais rápido, o que leva a um aumento da resistência da membrana. Assim, torna-se mais difícil para os íons hidrônio passarem através da membrana. Isto pode alterar o potencial de equilíbrio do eletrodo, causando uma mudança na leitura do pH.
Para medições de pH em temperaturas mais altas, use um eletrodo de pH com membrana de vidro «U» de cor verde, pois são mais tolerantes ao calor.
- Exemplo: Unidade Metrohm (figura 1)

Medições de pH em Baixas temperaturas mostram efeitos semelhantes. Em temperaturas mais baixas, a membrana torna-se mais rígida e o transporte de íons também é mais difícil. Além disso, a atividade dos íons hidrogênio na solução eletrolítica diminui em baixas temperaturas. Ambos os efeitos resultam num aumento da resistência da membrana.
Grosso modo, quando a solução de medição é resfriada em 10 K, a resistência da membrana dobra [1,2].
Para medições de pH em temperaturas mais baixas, recomenda-se um eletrodo com membrana de vidro «T» de cor azul e um eletrólito de referência espessado, pois o eletrólito de referência contém solventes que atuam como anticongelante.
- Exemplo: Metrohm Porotrode (Figura 2)
Posicionamento correto do sensor de temperatura e do eletrodo de pH
Certifique-se de que o sensor de temperatura esteja posicionado próximo à membrana de vidro do eletrodo de pH. Caso contrário, a temperatura da solução de medição não poderá ser medida corretamente.
Além disso, a compensação de pH estará incorreta, pois a temperatura e o pH não são medidos no mesmo local.
Para evitar completamente este efeito, utilize um eletrodo de pH com sensor de temperatura integrado. Neste caso, o sensor de temperatura está localizado dentro do eletrodo, nas imediações da membrana de vidro (Figura 3).
Eletrodos de pH combinados com sistema de referência «Long Life»
A maioria dos eletrodos de pH disponíveis no mercado são eletrodos de pH combinados com o sistema de referência Ag/AgCl. O produto de solubilidade do cloreto de prata depende da temperatura.
O produto de solubilidade do cloreto de prata em água é muito pequeno, aproximadamente 10-10 mol2/EU2. No entanto, o cloreto de prata dissolve-se muito facilmente sob formação de complexos. O aumento da temperatura favorece este efeito, resultando numa alteração do equilíbrio entre o cloreto de prata sólido e dissolvido. Portanto, se a temperatura mudar, é necessário esperar até que um equilíbrio estável seja alcançado novamente, pois esse equilíbrio determina o potencial do eletrodo de referência.
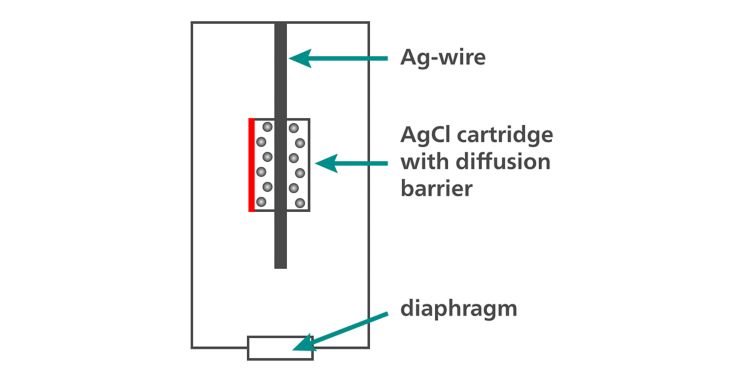
Graças ao sistema de referência «Long Life» utilizado nos eletrodos de pH Metrohm (Figura 4), o equilíbrio termodinâmico entre prata, cloreto de prata (sólido) e cloreto de prata (dissolvido) é estabelecido muito rapidamente e o potencial do eletrodo de referência torna-se estável após um tempo muito curto.
Calibração do eletrodo de pH
Os eletrodos de pH Metrohm são construídos de acordo com DIN 19263. Esses eletrodos exibem uma leitura de potencial de 0 mV (Zero pontos) em torno de pH 7. Conforme explicado anteriormente, de acordo com a equação de Nernst, a inclinação do eletrodo e (sob certas circunstâncias) também o deslocamento do ponto zero do eletrodo quando o eletrodo de pH é exposto a uma mudança de temperatura.
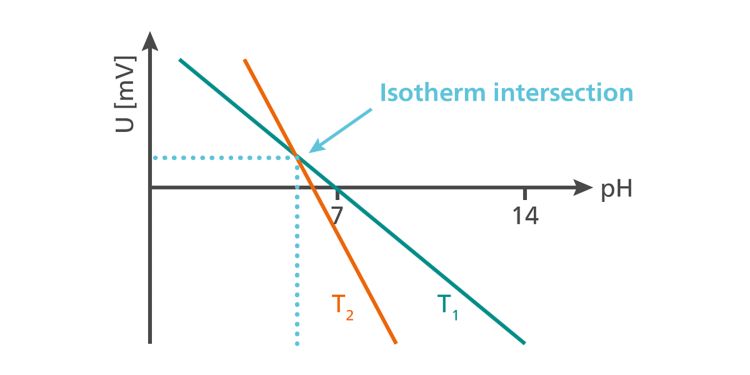
Considerando as curvas de calibração (isotermas) dos eletrodos de pH em diferentes temperaturas sob condições ideais, seria de esperar que elas se cruzassem no ponto zero do eletrodo. Infelizmente, este não é o caso dos eletrodos de pH na vida real. Um ponto de interseção isotérmico é formado (Figura 5) próximo ao ponto zero do eletrodo. A proximidade depende da condição do eletrodo.
Para minimizar tais efeitos, a calibração do eletrodo de pH deve ser realizada no mesma temperatura como será usado para medições de pH subsequentes.
Temperatura das soluções de medição
O valor do pH da água pura a 25 °C é 7,00. Neste caso, há números iguais de íons hidrônio e hidróxido presentes na água. Devido à dependência do produto iônico da água com a temperatura, esse equilíbrio muda para um pH mais alto em temperaturas mais baixas e vice-versa. Estas mudanças de equilíbrio são conhecidas para soluções tampão e para ácidos e bases bem conhecidos (ver mesa 2 por exemplo), mas não para todos os tipos de soluções de amostra.
Mesa 2. Três exemplos que mostram como as mudanças na temperatura podem afetar o valor do pH da amostra [3].
| pH de soluções medidas em diferentes temperaturas | 0°C | 25ºC | 50ºC |
|---|---|---|---|
| H2Ó | 7,47 | 7,00 | 6,63 |
| c = 0,001 mol/L HCl * | 3,00 | 3,00 | 3,00 |
| c = 0,001 mol/L NaOH | 11,94 | 11,00 | 10,26 |
* Os efeitos da temperatura são mais fracos em relação à determinação do pH de substâncias ácidas. Há uma tendência geral de aumento do valor do pH com o aumento da temperatura nestes casos.
Mesmo os medidores de pH mais modernos só podem corrigir o comportamento da temperatura do eletrodo, mas nunca o das soluções a serem medidas. Para medições corretas de pH, é essencial medir sempre o valor de pH de suas amostras na temperatura em que foram amostradas. Por exemplo, se uma amostra for coletada a 10 °C, a calibração do eletrodo de pH e a medição da amostra também deverão ser feitas a 10 °C. Seguir este protocolo ajuda a evitar efeitos indesejados de equilíbrio térmico e resulta em uma resposta mais rápida do eletrodo de pH.
Conclusão
Devido à sua construção otimizada, o comportamento real dos eletrodos de pH Metrohm de alta qualidade desvia-se apenas ligeiramente (potenciais de assimetria máximos +/- 15 mV) dos valores ideais. No entanto, como a maioria das coisas, mais de um fator está em jogo.
A lista de verificação abaixo pode ajudá-lo a obter resultados de medição precisos durante a calibração e medição de pH. Se você puder responder SIM a todos os pontos listados, a maioria dos efeitos causados pelas mudanças de temperatura serão considerados.
| SIM NÃO | |
|---|---|
| ( ) | Escolhi um eletrodo de vidro de pH apropriado considerando seu tipo de membrana de vidro para minha aplicação. |
| ( ) | Meu eletrodo de vidro de pH combinado está equipado com um sistema de referência «Long Life». |
| ( ) | Meu sensor de temperatura está posicionado próximo à membrana de vidro do meu eletrodo de pH. OU Estou usando um eletrodo de vidro de pH combinado com sensor de temperatura integrado para minha calibração/medição de pH. |
| ( ) | Meu medidor de pH possui compensação de temperatura integrada. |
| ( ) | Minha calibração é realizada na mesma temperatura de todas as medições de pH subsequentes. |
| ( ) | Todas as soluções de amostra a serem medidas estão à mesma temperatura. |
Referências
[1] Degner, R.; Leibl, S. PH Messen: Então o Gemacht de Wird!; Wiley, 1995.
[2] Galster, H. PH-Messung: Grundlagen, Methoden, Anwendungen, Geräte; VCH, 1990.
[3] pH e temperatura – dois untrennbare Größen. Ciência Analítica Wiley. https://analyticalscience.wiley.com/do/10.1002/was.00050234 (acessado em 09/02/2023).
 Compartilhar artigo
Compartilhar artigo